INTRODUCTION
La bronchopneumopathie chronique obstructive (BPCO) est une maladie respiratoire définie par une obstruction chronique du débit aérien. Elle inclut les diagnostics d’emphysème - destruction étendue et irréversible des parois alvéolaires – et de bronchite chronique obstructive, de nombreuses personnes présentant ces deux affections.
Témoignant d’un fort enjeu de santé publique, cette affection a fait l’objet du premier parcours de soins copiloté par la Haute Autorité de santé (HAS) et la Caisse nationale d’assurance maladie (Cnam) dans le cadre de Ma santé 2022 (2). Alors qu'au moins les deux tiers des patients atteints de BPCO ne seraient pas diagnostiqués, l’accent est mis sur la détection précoce de cette maladie et sa prise en charge globale.
ÉPIDÉMIOLOGIE
La prévalence de la BPCO est difficile à estimer en raison du sous-diagnostic et de la difficulté à réaliser des épreuves fonctionnelles respiratoires (EFR) dans le cadre d’études épidémiologiques. Elle est cependant estimée à̀ 7,5 % dans une population de plus de 45 ans.
Au niveau mondial, plus de 480 millions de personnes seraient actuellement atteintes. Et si rien ne change, dans moins d’une génération, en 2050, ce seront près de 600 millions de personnes qui en souffriront, avec une part croissante de femmes impactées. En effet, si l’incidence semble se stabiliser chez l’homme, elle croît chez la femme (3).
Le tabagisme est retrouvé dans plus de 70 % des cas de BPCO dans les pays à revenu élevé et dans 30 à 40 % des cas dans les pays à revenu faible ou intermédiaire, derrière la pollution de l’air intérieur (1).
En France, la BPCO est un problème de santé publique avec plus de trois millions de patients concernés (4). À cette prévalence importante et croissante s’ajoute la problématique du sous-diagnostic : selon la HAS, entre 66 et 90 % des personnes atteintes ne sont pas diagnostiquées (2).
Par ailleurs, le poids des pathologies concomitantes est considérable dans la BPCO. Une récente étude conduite à partir de la base de données IQVIA (juillet 2021 - juin 2022 ; 1 300 000 patients traités pour BPCO) (5) a montré que parmi ces patients 57 % avaient reçu un traitement pour insuffisance cardiaque (IC) et 47 % pour une pathologie cardiovasculaire (hors IC). Par ailleurs, 19 % étaient traités pour diabète et 41 % pour anxiété/dépression/pathologie psychiatrique. Plus de la moitié de ces personnes souffrant de BPCO avait présenté au moins une exacerbation modérée dans les 12 derniers mois. 13 % des exacerbations étaient traitées par corticostéroïdes oraux (CSO). 46 % des patients recevaient un antibiotique et 41 % étaient sous CSO et antibiotique. Seuls 13 % avaient consulté un pneumologue, 63 % un médecin généraliste et 24 %, les deux.
DÉTECTER LA BPCO
L’éventualité d’une BPCO doit être évoquée en consultation dès lors qu’un patient a plus de 40 ans et est potentiellement à risque (tabagisme, consommation de cannabis, profession exposée, pollution…) et/ou symptomatique (dyspnée, toux, expectoration, bronchites à répétition…).
Tout professionnel de santé doit penser à la BPCO, y compris chez l’adulte jeune, et poser la question des facteurs de risque et des symptômes précoces.
Concernant les facteurs de risque, le dépistage du tabagisme doit conduire à rechercher les pathologies associées à la consommation de tabac (BPCO, insuffisance respiratoire et coronarienne, pathologie vasculaire) et être complété par la recherche de facteurs environnementaux, dont les pollutions atmosphérique et intérieure (chauffage au bois ou charbon notamment), et exposition professionnelle à des toxiques ou à des irrita nts : particules minérales (silice, charbon) ou organiques (végétales, moisissures),gaz, vapeurs et fumées.
Le symptôme majeur de la BPCO est la dyspnée, qui induit une réduction de l’activité physique quotidienne. Peu de patients s’en aperçoivent car celle-ci est d’apparition progressive.
> Dépister la BPCO en 5 questions
La HAS met à la disposition des patients un questionnaire d’administration rapide adapté à la médecine de premier recours (et en autodépistage) pour repérer les premiers symptômes d’une BPCO (6) :
- Toussez-vous souvent (tous les jours) ? : oui ❏ non ❏
- Avez-vous souvent une toux grasse qui ramène des crachats ? : oui ❏ non ❏
- Êtes-vous plus facilement essouflé que les personnes de votre âge ? : oui ❏ non ❏
- Avez-vous fumé ou fumez-vous ? : oui ❏ non ❏
Deux réponses OUI constituent un signal d’alerte. Avec trois réponses positives à ces questions, le médecin généraliste peut soit effectuer une spirométrie, soit orienter le patient vers un pneumologue.
DIAGNOSTIC
Devant une suspicion de BPCO, pratiquer une spirométrie chez un patient à l’état stable (à distance d’un épisode aigu de bronchite ou d’exacerbation) peut mettre en évidence un trouble ventilatoire obstructif non réversible après bronchodilatateur.
La spirométrie mesure les volumes d’air mobilisés par les mouvements respiratoires et les débits ventilatoires. Elle permet de mesurer la capacité vitale forcée (CVF) et le volume expiratoire maximal à la première seconde (VEMS). Un rapport VEMS/CVF < 70 % après inhalation d’un bronchodilatateur (test de réversibilité) permet de poser le diagnostic de BPCO.
Attention, ce critère peut conduire à un sous-diagnostic de l’obstruction bronchique chez les patients de moins de 50 ans, et surtout à un surdiagnostic chez les patients plus âgés. L’alternative est une définition de l’obstruction bronchique fondée sur un VEMS/CVF < limite inférieure de la normale (LIN) pour la classe d’âge considérée.
Si le rapport VEMS/CVF est compris entre 60 et 80 %, la spirométrie sera répétée.
Pour sa part, la pléthysmographie permet de mesurer les volumes pulmonaires non mobilisables : volumes d’air restant après une expiration passive - capacité résiduelle fonctionnelle - et après une expiration maximale - volume résiduel. La mesure des volumes non mobilisables permet de calculer la capacité pulmonaire. Cet examen permet donc de dépister une distension dynamique associée au trouble ventilatoire obstructif, définie par une augmentation des volumes non mobilisables au détriment des volumes mobilisables. Cette distension est souvent présente lors de lésions emphysémateuses associées et est généralement mieux corrélée à la dyspnée que le simple VEMS.
Une radiographie du thorax est indispensable à la recherche de lésions évoquant une anomalie cardiaque, pulmonaire ou pleurale, un cancer du poumon. D’autres examens peuvent être pratiqués. D’un point de vue biologique : NFS, glycémie et bilan lipidique sont systématiques.
Le pneumologue peut être consulté pour confirmer le diagnostic, pour évaluer la sévérité de la maladie et son contrôle en cas de dissociation entre la clinique et les signes fonctionnels ou de suspicion de forme sévère ou très sévère (stades III et IV), ou encore, en cas d’exacerbations fréquentes (> à 2 par an) ou sévère (hospitalisation) ou de comorbidités.
ÉVALUER LA SÉVÉRITÉ
La sévérité de la maladie dépend de plusieurs facteurs, dont la sévérité de l’obstruction bronchique (voir ci-dessous), l’importance du tabagisme, la sévérité de la dyspnée ou de l’incapacité, l’état nutritionnel, le nombre d’exacerbations et le handicap lié à la BPCO.
> Stades de la BPCO selon l'obstruction bronchique
Chez les patients ayant un rapport VEMS/CVF < 70 %, la valeur du VEMS permet de déterminer le stade de la maldie :
- Stade I (léger) : VEMS ≥ 80 % de la valeur prédite (valeur attendue en tenant compte de l’âge, du sexe, de la taille et de l’origine ethnique .
- Stade II (modéré) : 50 % ≤ VEMS < 80 % valeur prédite.
- Stade III (sévère) : 30 % ≤ VEMS < 50 % valeur prédite.
- Stade IV (très sévère) : VEMS < 30 % valeur prédite ou VEMS < 50 % valeur prédite avec insuffisance respiratoire chronique grave.
L’évaluation de la sévérité de l’état du patient inclut également la recherche de comorbidités : pathologies cardiovasculaires (consultation d’un cardiologue recommandée dans l’année post-diagnostic) ; syndrome des apnées obstructives du sommeil ; dénutrition, fonte musculaire ; ostéoporose ; dépression et/ou anxiété ; co-addictions ; diabète ; anémie ; reflux gastro-œsophagien.
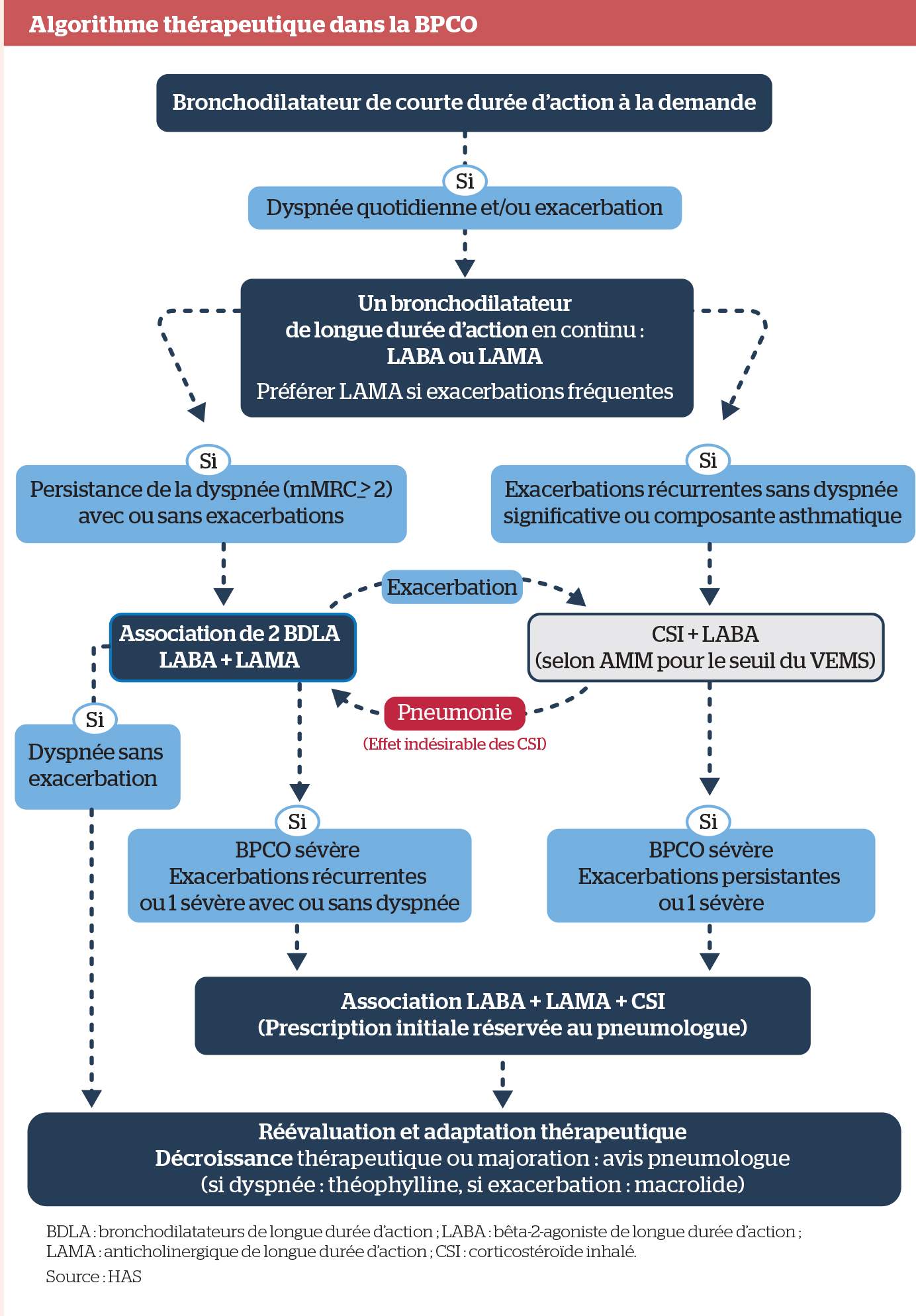
TRAITEMENT (hors exacerbation)
Le traitement symptomatique comprend les bronchodilatateurs (BD) administrés par voie inhalée : BD de courte durée d’action en cas de symptôme épisodique puis, si dyspnée quotidienne et/ou exacerbations récurrentes, BD de longue durée d’action en monothérapie et, si échec, en association.
Le choix du dispositif d’inhalation dépend de la capacité du patient et de sa préférence. Son bon maniement doit être expliqué au patient et vérifié avec lui. D’après une enquête de Santé respiratoire France qui confirme les données de la littérature, près de la moitié des patients n’utilisent pas correctement leur inhalateur (7).
Il n’y a pas d’indication aux corticoïdes inhalés en monothérapie, en traitement de fond ou en phase d’exacerbation (absence d’AMM) ; ils ne sont indiqués qu’en association à un bêta-2-agoniste de longue durée d’action en cas d’antécédents d’exacerbations répétées et de symptômes significatifs malgré un traitement bronchodilatateur continu et selon l’indication de l’AMM (seuil du VEMS variable) (2).
> À ne pas oublier :
Au-delà du traitement médicamenteux respiratoire :
- Intervenir à chaque entretien pour favoriser et maintenir le sevrage tabagique.
- Vacciner contre la grippe annuellement et contre le pneumocoque.
- Encourager la pratique d’une activité physique régulière et éventuellement orienter vers une activité physique adaptée (APA).
- Proposer la réadaptation respiratoire dès la présence d’une dyspnée, d’une intolérance à l’exercice ou d’une diminution des activités quotidiennes.
Pour les patients insuffisants respiratoires, la prise en charge régulière par le pneumologue est impérative (mise en place d’une oxygénothérapie de longue durée, coordination des différents professionnels). Le généraliste intervient en support dans la surveillance de l’efficacité, de la tolérance et de l’observance des traitements. L’oxygène doit être administré au moins 15 h par jour (impact sur la survie) avec l’objectif d’une PaO2 au repos > 60 mmHg et/ou une SpO2 > 90 %.
SUIVI DU PATIENT
Chez tous les patients, quel que soit le stade de sévérité, le suivi est clinique, portant sur la dyspnée (échelle mMRC, voir ci-dessous), la toux, la présence de crachats, le nombre d’exacerbations/an, le sevrage tabagique, l’activité physique, la qualité de vie, le suivi nutritionnel (dont le poids).
Échelle de dyspnée du Medical Research Council modifiée (mMRC) :

À chaque consultation, la mesure de la saturation pulsée en oxygène (SpO2) et un test de marche de 6 minutes ou autre test de capacité à l’exercice sont préconisés.
Les comorbidités sont à rechercher régulièrement, à explorer et à traiter.
Concernant les traitements médicamenteux, l’observance, les effets indésirables et les techniques d’inhalation sont à surveiller à chaque consultation, et à réévaluer entre 1 et 3 mois après chaque changement. L’éducation thérapeutique du patient est individuelle ou collective.
La mise en ALD 14 doit être déclenchée en cas de VEMS < 50 %, ainsi que la déclaration de maladie professionnelle le cas échéant.
La réalisation d’EFR (VEMS et capacité vitale forcée/CVF) se fera à un rythme adapté à l’état clinique du patient, généralement 1 fois par an pour les patients dont la BPCO est de stade I à III. Ceux dont la BPCO est de stade IV doivent être évalués par le pneumologue, qui adaptera le rythme des EFR. Une spirométrie peut également être indiquée après un changement thérapeutique et doit être réalisée à distance d’une exacerbation (3 mois au minimum).
D’autres examens peuvent être nécessaires selon le contexte et l’état clinique du patient : ECBC, radiographie de thorax, tomodensitométrie, endoscopie, explorations fonctionnelles d’exercice, pléthysmographie à la recherche d’une distension thoracique, oxymétrie nocturne, capnographie nocturne, poly(somno)graphie, échographie cardiaque. Le recours au médecin physique et de réadaptation est préconisé en cas de comorbidité, notamment locomotrice ou neurologique, gênant la mise en place d’une activité physique (cardiologue et autres spécialistes selon les comorbidités).
Au décours d’une hospitalisation pour décompensation, une consultation de médecine générale doit être programmée dans la semaine qui suit la sortie, et du pneumologue dans les 1 à 2 mois avec gaz du sang et spirométrie. À la suite d’un séjour en réanimation ou soins intensifs, une consultation avec un pneumologue doit être réalisée dans les 4 semaines et, si l’état de base n’est pas atteint, des consultations supplémentaires s’ajoutent. Selon l’évolution, des EFR doivent être programmées à 3 mois et à 1 an.
> Rythme de consultation selon le stade de gravité :
- Absence d’exacerbation, dyspnée absente ou légère (mMRC 0-1) ou < 2 exacerbations modérées/an, dyspnée modérée (mMRC 2) :
Médecin généraliste : consultations dédiées à la BPCO au moins 1 fois par an
Avis du pneumologue : selon les besoins
- ≥ 2 exacerbations modérées ou 1 sévère (hospitalisation)/an, dyspnée sévère (mMRC 3-4), patient sans oxygénothérapie de longue durée :
Médecin généraliste : au moins 2 fois par an
Pneumologue : 1 fois par an
- Patient sous oxygénothérapie de longue durée et/ou ventilation non invasive à l’état stable :
Médecin généraliste : tous les mois
Pneumologue : tous les 6 mois
Prestataire : selon le forfait, à adapter si besoin
EN RÉSUMÉ
- Repérer la BPCO en posant la question du tabagisme et des autres facteurs de risque à tous les patients, notamment de plus de 40 ans.
- En cas de symptôme ou de facteur de risque, faire une spirométrie avec test de réversibilité pour poser le diagnostic de BPCO.
- Demander l’avis du pneumologue en cas de doute diagnostique ou de discordance avec la clinique (emphysème prédominant).
- Le traitement symptomatique repose sur les bronchodilatateurs par voie inhalée, de courte et/ou de longue durée d’action, selon la clinique. Ne pas traiter les patients ayant une BPCO par des corticostéroïdes inhalés en monothérapie.
- Le maniement du dispositif d’inhalation doit être expliqué au patient puis vérifié à chaque occasion.
- Le sevrage tabagique, l’activité physique et les vaccinations antigrippale et antipneumococcique sont indispensables pour la prise en charge de la BPCO.
- La réadaptation respiratoire doit être proposée à tout patient dyspnéique.
Hélène Joubert (rédactrice) avec le Dr Frédéric le Guillou (pneumologue, Le Pradet, président de Santé respiratoire France)
BIBLIOGRAPHIE
1. OMS. La bronchopneumopathie obstructive. 16 mars 2023. https://www.who.int/fr/news-room/fact-sheets/detail/chronic-obstructive…-(copd)
2. HAS. Guide du parcours de soins. Bronchopneumopathie chronique obstructive. Actualisation Novembre 2019.
3. Boers E., Barrett M., Vuong V. et al. Late Breaking Abstract - An estimate of the global COPD prevalence in 2050 : Disparities by income and gender. Congrès ERS 2022
3. Fuhrman C, Delmas M. Épidémiologie descriptive de la bronchopneumopathie chronique obstructive (BPCO) en France. Rev Mal Resp 2010 ;27(2).
5. Intervention du Pr Nicolas Roche au 27e Congrès CPLF 2023.
6. Autoquestionnaire. Dépistage BPCO adapté de la Global initiative for Chronic Obstructive Lung Disease, 2014.
7. Enquête Living Lab Santé respiratoire France, « Formation des patients BPCO à l’utilisation des inhalateurs ». REspilab, poster Congrès CPLF 2020.
Liens d'intérêts : L'auteur déclare n'avoir aucun lien d'intérêts relatif au contenu de cet article


Mise au point
Troubles psychiatriques : quand évoquer une maladie neurodégénérative ?
Étude et pratique
Complications de FA, l’insuffisance cardiaque plus fréquente que l’AVC
Cas clinique
L’ictus amnésique idiopathique
Recommandations
Antibiothérapies dans les infections pédiatriques courantes (2/2)